DDT (Dichloro-Diphenyl-Trichloroethane) adalah salah satu yang dikenal pestisida sintetis. Ini merupakan bahan kimia yang panjang, unik, dan sejarah kontroversial.
Synthesized pertama di 1874, DDT’s insecticidal properti tidak ditemukan sampai 1939. Dalam paruh kedua Perang Dunia II, telah digunakan dengan dampak yang luar biasa di antara kedua-dua penduduk sipil dan militer untuk mengendalikan penyebaran nyamuk malaria dan kutu transmisi tipus, mengakibatkan penurunan dramatis dalam insiden kedua penyakit. Swiss chemist Paul Hermann Müller dari Geigy Pharmaceutical dianugerahi Penghargaan Nobel dalam Physiology Pengobatan atau di 1948 “untuk penemuan tingginya efisiensi DDT sebagai racun kontak terhadap beberapa arthropods Setelah perang, DDT telah tersedia untuk digunakan sebagai insektisida pertanian, dan segera produksinya dan menggunakan skyrocketed.
Pada tahun 1962, Silent Spring oleh American biologi Rachel Carson telah diterbitkan. Buku di katalog lingkungan dampak dari sembarangan penyemprotan DDT di Amerika Serikat dan pertanggungjawaban logika melepaskannya dari banyak bahan kimia ke dalam lingkungan tanpa sepenuhnya pemahaman mereka terhadap ekologi atau kesehatan manusia. Buku yang disarankan DDT dan pestisida dapat menyebabkan kanker dan pertanian yang mereka gunakan merupakan ancaman bagi satwa liar, terutama burung. Publikasi-nya adalah salah satu tanda tangan dalam peristiwa kelahiran gerakan lingkungan hidup. Diam Spring menghasilkan besar masyarakat yang gaduh akhirnya menyebabkan paling pantas atas DDT yang dilarang di AS pada 1972. [4] DDT kemudian dilarang digunakan untuk pertanian di seluruh dunia di bawah Konvensi Stockholm, namun terbatas dalam menggunakan penyakit vector kontrol terus
Seiring dengan petikan dari Endangered Species Act, Amerika Serikat pada ban DDT adalah dikutip oleh para ilmuwan sebagai faktor utama dalam cerdas dari bald eagle berdampingan di Amerika Serikat.
DDT adalah insektisida organochlorine, mirip dalam struktur ke dicofol dan pestisida methoxychlor. Ini adalah sangat hydrophobic, warna, kristal kuat dengan yang lemah, bau kimia. Yg tdk dpt ia hampir dalam air tetapi kelarutan yang baik di sebagian besar larutan organik, Fats, dan minyak. DDT tidak terjadi secara alami, namun yang dihasilkan oleh reaksi dari khloral (CCl3CHO) dengan chlorobenzene (C6H5Cl) di hadapan sulfuric acid, yang bertindak sebagai katalisator. DDT nama dagang yang telah dipasarkan di bawah termasuk Anofex, Cezarex, Chlorophenothane, Clofenotane, Dicophane, Dinocide, Gesarol, Guesapon, Guesarol, Gyron, Ixodex, Neocid, Neocidol, dan Zerdane.
Isomer dan Terkait
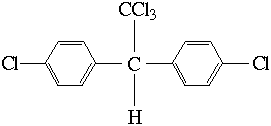
DDT komersial sebenarnya campuran dari beberapa erat kaitannya compounds. Komponen utama (77%) adalah p, p isomer yang digambarkan di atas artikel ini. , O, p ‘isomer (digambarkan di sebelah kanan) juga hadir dalam jumlah yang signifikan (15%). Dichlorodiphenyldichloroethylene (DDE) dan dichlorodiphenyldichloroethane (es) membentuk keseimbangan. DDD DDE dan juga yang besar dan metabolites kemogokan produk DDT di lingkungan. [3] Istilah “total DDT” sering digunakan untuk merujuk kepada jumlah semua terkait DDT compounds (p, p-DDT, o, p – DDT, DDE,dan pakaian dalam sampel.
Mekanisme aksi
DDT adalah racun cukupan, dengan tikus LD50 dari 113 mg / kg. [12] Hal ini berpengaruh insecticidal properti, dimana kills membuka saluran ion sodium di neurons, sehingga mereka ke api yang mengarah ke spasms spontan dan akhirnya mati. Serangga tertentu dengan mutations di saluran sodium gene yang tahan terhadap DDT dan insektisida sejenis lainnya. DDT tahan juga conferred oleh up-peraturan mengekspresikan gen cytochrome P450 dalam beberapa jenis serangga.
DDT (Dichloro Diphenyl Trichlorethane) adalah insektisida “tempo dulu” yang pernah disanjung “setinggi langit” karena jasa-jasanya dalam penanggulangan berbagai penyakit yang ditularkan vektor serangga. Tetapi kini penggunaan DDT di banyak negara di dunia terutama di Amerika Utara, Eropah Barat dan juga di Indonesia telah dilarang. Namun karena persistensi DDT dalam lingkungan sangat lama, permasalahan DDT masih akan berlangsung pada abad 21 sekarang ini. Adanya sisa (residu) insektisida ini di tanah dan perairan dari penggunaan masa lalu dan adanya bahan DDT sisa yang belum digunakan dan masih tersimpan di gudang tempat penyimpanan di selurun dunia (termasuk di Indonesia) kini menghantui mahluk hidup di bumi. Bahan racun DDT sangat persisten (tahan lama, berpuluh-puluh tahun, bahkan mungkin sampai 100 tahun atau lebih?), bertahan dalam lingkungan hidup sambil meracuni ekosistem tanpa dapat didegradasi secara fisik maupun biologis, sehingga kini dan di masa mendatang kita masih terus mewaspadai akibat-akibat buruk yang diduga dapat ditimbulkan oleh keracunan DDT.
Sifat kimiawi dan fisik DDT
Senyawa yang terdiri atas bentuk-bentuk isomer dari 1,1,1-trichloro-2,2-bis-(p-chlorophenyl) ethane yang secara awam disebut juga Dichoro Diphenyl Trichlorethane (DDT) diproduksi dengan menyampurkan chloralhydrate dengan chlorobenzene.
DDT pertama kali disintesis oleh Zeidler pada tahun 1873 tapi sifat insektisidalnya baru ditemukan oleh Dr Paul Mueller pada tahun 1939. Penggunaan DDT menjadi sangat populer selama Perang Dunia II, terutama untuk penanggulangan penyakit malaria, tifus dan berbagai penyakit lain yang ditularkan oleh nyamuk, lalat dan kutu. Di India, pada tahun 1960 kematian oleh malaria mencapai 500.000 orang turun menjadi 1000 orang pada tahun 1970. WHO memperkirakan bahwa DDT selama Perang Dunia II telah menyelamatkan sekitar 25 juta jiwa terutama dari ancaman malaria dan tifus, sehingga Paul Mueller dianugerahi hadiah Nobel dalam ilmu kedokteran dan fisiologi pada tahun 1948.
DDT adalah insektisida paling ampuh yang pernah ditemukan dan digunakan manusia dalam membunuh serangga tetapi juga paling berbahaya bagi umat manusia manusia sehingga dijuluki “The Most Famous and Infamous Insecticide”.
Bahaya toksisitas DDT terhadap ekosistem
Pada tahun 1962 Rachel Carson dalam bukunya yang terkenal, Silenty Spring menjuluki DDT sebagai obat yang membawa kematian bagi kehidupan di bumi. Demikian berbahayanya DDT bagi kehidupan di bumi sehingga atas rekomendasi EPA (Environmental Protection Agency) Amerika Serikat pada tahun 1972 DDT dilarang digunakan terhitung 1 Januari 1973. Pengaruh buruk DDT terhadap lingkungan sudah mulai tampak sejak awal penggunaannya pada tahun 1940-an, dengan menurunnya populasi burung elang sampai hampir punah di Amerika Serikat. Dari pengamatan ternyata elang terkontaminasi DDT dari makanannya (terutama ikan sebagai mangsanya) yang tercemar DDT. DDT menyebabkan cangkang telur elang menjadi sangat rapuh sehingga rusak jika dieram. Dari segi bahayanya, oleh EPA DDT digolongkan dalam bahan racun PBT (persistent, bioaccumulative, and toxic) material.
Dua sifat buruk yang menyebabkan DDT sangat berbahaya terhadap lingkungan hidup adalah:
Sifat apolar DDT: ia tak larut dalam air tapi sangat larut dalam lemak. Makin larut suatu insektisida dalam lemak (semakin lipofilik) semakin tinggi sifat apolarnya. Hal ini merupakan salah satu faktor penyebab DDT sangat mudah menembus kulit
Sifat DDT yang sangat stabil dan persisten. Ia sukar terurai sehingga cenderung bertahan dalam lingkungan hidup, masuk rantai makanan (foodchain) melalui bahan lemak jaringan mahluk hidup. Itu sebabnya DDT bersifat bioakumulatif dan biomagnifikatif.
Karena sifatnya yang stabil dan persisten, DDT bertahan sangat lama di dalam tanah; bahkan DDT dapat terikat dengan bahan organik dalam partikel tanah.
Dalam ilmu lingkungan DDT termasuk dalam urutan ke 3 dari polutan organik yang persisten (Persistent Organic Pollutants, POP), yang memiliki sifat-sifat berikut:
tak terdegradasi melalui fotolisis, biologis maupun secara kimia,
-berhalogen (biasanya klor),
-daya larut dalam air sangat rendah,
-sangat larut dalam lemak,
-semivolatile,
-di udara dapat dipindahkan oleh angin melalui jarak jauh,
-bioakumulatif,
-biomagnifikatif (toksisitas meningkat sepanjang rantai makanan)
Di Amerika Serikat, DDT masih terdapat dalam tanah, air dan udara: kandungan DDT dalam tanah berkisar sekitar 0.18 sampai 5.86 parts per million (ppm), sedangkan sampel udara menunjukkan kandungan DDT 0.00001 sampai 1.56 microgram per meter kubik udara (ug/m3), dan di perairan (danau) kandungan DDT dan DDE pada taraf 0.001 microgram per liter (ug/L). Gejala keracunan akut pada manusia adalah paraestesia, tremor, sakit kepala, keletihan dan muntah. Efek keracunan kronis DDT adalah kerusakan sel-sel hati, ginjal, sistem saraf, system imunitas dan sistem reproduksi. Efek keracunan kronis pada unggas sangat jelas antara lain terjadinya penipisan cangkang telur dan demaskulinisasi
Sejak tidak digunakan lagi (1973) kandungan DDT dalam tanaman semakin menurun. Pada tahun 1981 rata-rata DDT dalam bahan makanan yang termakan oleh manusia adalah 32-6 mg/kg/hari, terbanyak dari umbi-umbian dan dedaunan. DDT ditemukan juga dalam daging, ikan dan unggas.
Walaupun di negara-negara maju (khususnya di Amerika Utara dan Eropah Barat) penggunaan DDT telah dilarang, di negara-negara berkembang terutama India, RRC dan negara-negara Afrika dan Amerika Selatan, DDT masih digunakan. Banyak negara telah melarang penggunaan DDT kecuali dalam keadaan darurat terutama jika muncul wabah penyakit seperti malaria, demam berdarah dsb. Departeman Pertanian RI telah melarang penggunaan DDT di bidang pertanian sedangkan larangan penggunaan DDT di bidang kesehatan dilakukan pada tahun 1995. Komisi Pestisida RI juga sudah tidak memberi perijinan bagi pengunaan pestisida golongan hidrokarbon-berklor (chlorinated hydrocarbons) atau organoklorin (golongan insektisida di mana DDT termasuk).
Permasalahan sekarang
Walaupun secara undang-undang telah dilarang, disinyalir DDT masih juga secara gelap digunakan karena keefektifannya dalam membunuh hama serangga. Demikian pula, banyaknya DDT yang masih tersimpan yang perlu dibinasakan tanpa membahayakan ekosistem manusia maupun kehidupan pada umumnya merupakan permasalahan bagi kita. Sebenarnya, bukan saja DDT yang memiliki daya racun serta persistensi yang demikian lamanya dapat bertahan di lingkungan hidup. Racun-racun POP lainnya yang juga perlu diwaspadai karena mungkin saja terdapat di tanah, udara maupun perairan di sekitar kita adalah aldrin, chlordane, dieldrin, endrin, heptachlor, mirex, toxaphene, hexachlorobenzene, PCB (polychlorinated biphenyls), dioxins dan furans.
Untuk mengeliminasi bahan racun biasanya berbagai cara dapat digunakan seperti secara termal, biologis atau kimia/fisik. Untuk Indonesia dipertimbangkan untuk mengadopsi cara stabilisasi/fiksasi karena dengan cara termal seperti insinerasi memerlukan biaya sangat tinggi. Prinsip stabilisasi/fiksasi adalah membuat racun tidak aktif/imobilisasi dengan enkapsulasi mikro dan makro sehingga DDT menjadi berkurang daya larutnya. Namun permasalahan tetap masih ada karena DDT yang telah di-imobilisasi ini masih harus “dibuang” sebagai landfill di tempat yang “aman”. Namun dengan cara ini potensi racun DDT masih tetap bertahan untuk waktu yang lama pada abad 21 ini.
BAHAYA DDT PADA MAKHLUK HIDUP
Pada bulan Juli 1998, perwakilan dari 120 negara bertemu untuk membahas suatu pakta Persatuan Bangsa Bangsa untuk melarang penggunaan DDT sebagai insektisida dan 11 bahan kimia lainnya secara global pada tahun 2000. Amerika Serikat dan negara-negara industri lain menyetujui pelarangan ini karena bahan-bahan kimia ini adalah senyawa kimia yang persisten dimana senyawa-senyawa ini dapat terakumulasi dan merusak ekosistem alami dan memasuki rantai makanan manusia. Namun banyak negara tidak setuju dengan pelarangan DDT secara global karena DDT digunakan untuk mengkontrol nyamuk penyebab malaria. Malaria timbul di 90 negara di seluruh dunia, termasuk Indonesia, dan merupakan penyebab kematian dalam jumlah besar terutama daerah ekuatorial Afrika.Organisasi Kesehatan Dunia memperkirakan bahwa 2.5 juta orang tewas setiap tahun akibat malaria dan ini kian terjadi di berbagai belahan dunia. Namun karena DDT begitu efektif dalam mengontrol nyamuk penyebab malaria, banyak ahli berpikir bahwa insektisida menyelamatkan lebih banyak jiwa dibandingkan bahan kimia lainnya.
DDT diproduksi secara massal pada tahun 1939, setelah seorang kimiawan bernama Paul Herman Moller menemukan dengan dosis kecil dari DDT maka hampir semua jenis serangga dapat dibunuh dengan cara mengganggu sistem saraf mereka. Pada waktu itu, DDT dianggap sebagai alternatif murah dan aman sebagai jenis insektisida bila dibandingkan dengan senyawa insektisida lainnya yang berbasis arsenik dan raksa. Sayangnya, tidak seorangpun yang menyadari kerusakan lingkungan yang meluas akibat pemakaian DDT.
Sebagai suatu senyawa kimia yang persisten, DDT tidak mudah terdegradasi menjadi senyawa yang lebih sederhana. Ketika DDT memasuki rantai makanan, ini memiliki waktu paruh hingga delapan tahun, yang berarti setengah dari dosis DDT yang terkonsumsi baru akan terdegradasi setelah delapan tahun. Ketika tercerna oleh hewan, DDT akan terakumulasi dalam jaringan lemak dan dalam hati. Karena konsentrasi DDT meningkat saat ia bergerak ke atas dalam rantai makanan, hewan predator lah yang mengalami ancaman paling berbahaya. Populasi dari bald eagle dan elang peregrine menurun drastis karena DDT menyebabkan mereka menghasilkan telur dengan cangkang yang tipis dimana telur ini tidak akan bertahan pada masa inkubasi. Singa laut di lepas pantai California akan mengalami keguguran janin setelah memakan ikan yang terkontaminasi.
Seperti yang terlihat pada diagram, DDT (diklorodifeniltrikloroetana) adalah senyawa hidrokarbon terklorinasi. Tiap heksagon dari struktur ini terdapat gugus fenil (C6H5-) yang memiliki atom klor yang mengganti satu atom hidrogen. Namun, perubahan kecil pada struktur molekularnya dapat membuat hidrokarbon terklorinasi ini aktif secara kimia.
Dengan memanipulasi molekul DDT dalam cara ini, kimiawan berharap untuk mengembangkan suatu insektisida yang efektif namun ramah lingkungan, dimana senyawa in akan mudah terdegradasi. Namun disaat bersamaan, para peneliti sedang menyelidiki cara lain untuk mengkontrol populasi nyamuk. Salah satu caranya adalah penggunaan senyawa menyerupai hormon yang menyebabkan nyamuk mati kelaparan, hingga dapat mengurangi populasinya hingga dapat mengurangi penyebaran malaria.
Para peneliti lingkungan dan pakar wabah penyakit mulai mengamati serius dampak unsur pengganggu itu sejak tiga dekade lalu. Mula-mula diketahui, racun pembunuh serangga yang amat ampuh dan digunakan secara luas membasmi nyamuk malaria, yakni DDT (dichlorodiphenytrichloroethane) memiliki dampak sampingan amat merugikan. DDT memiliki sifat larut dalam lemak. Karena itu, residunya terus terbawa dalam rantai makanan, dan menumpuk dalam jaringan lemak. Dari situ, sisa DDT mengalir melalui air susu ibu kepada anaknya, baik pada manusia maupun pada binatang. Binatang pemangsa mendapat timbunan sisa DDT dari binatang makanannya. Rantainya seolah tidak bisa diputus.
Pengamatan terhadap burung pemangsa menunjukkan, DDT menyebabkan banyak burung yang memproduksi telur dengan kulit amat tipis, sehingga mudah pecah. Selain itu, terlepas dari tebal tipisnya kulit telur, semakin banyak anak burung pemangsa yang lahir cacat. Penyebaran residu DDT bahkan diamati sampai ke kawasan kutub utara dan selatan. Anjing laut di kutub utara, banyak yang melahirkan anak yang cacat, atau mati pada saat dilahirkan. Penyebabnya pencemaran racun serangga jenis DDT.
Diduga, residu DDT pada manusia juga berfungsi serupa, yakni menurunkan kemampuan reproduksi. Atau menyebabkan cacat pada janin.